Die gemeinsame Ursache aller chronischen Entzündungen liegt in einem fehlgeleiteten Immunsystem – unser Immunsystem ist sprichwörtlich aus der Bahn geraten.
Doch wann kommt es eigentlich zu einer Autoimmunerkrankung und wann zu Allergien? Was ist der Unterschied zwischen Neurodermitis und Psoriasis? Warum schlägt eine bestimmte Therapie bei jemandem gut an und bei jemand anderem nicht?
Damit du die Gründe dafür besser verstehen kannst, möchte ich dir in diesem Artikel das sogenannte TH1/TH2-Immunbalance-Modell vorstellen. Werfen wir dafür zunächst einen näheren Blick auf unser Immunsystem.
Das angeborene und das erworbene Immunsystem
Unser Immunsystem setzt sich im Wesentlichen aus zwei Teilen zusammen: einem unspezifischen (angeborenen) Immunsystem und einem spezifischen (erworbenen) Immunsystem.
Das unspezifische Immunsystem ist bereits bei der Geburt vorhanden. Eine der ersten Schutzbarrieren für potentielle Krankheitserreger sind dabei unsere Haut und Schleimhäute. Unser Darm stellt mit einer Oberfläche von 400 -500 Quadratmeter das größte Immunorgan des Körpers dar. Falls Erreger diese Barrieren überwinden, bilden bestimmte weiße Blutzellen (Phagozyten) die erste Abwehr. Auch körpereigene Botenstoffe, die von den Zellen des Immunsystems gebildet werden, wirken an der unspezifischen Abwehr mit (humorale Immunabwehr).
Das unspezifische Immunsystem antwortet schnell und reagiert aber auf alle Krankheitserreger gleich. Daher bedarf es oft noch einer effektiveren Immunantwort und die spezifische Immunantwort wird ebenfalls eingeleitet. Sie benötigt jedoch Stunden und Tage, um die volle Effektivität zu erreichen. Dafür zeichnet sie sich durch eine große Anpassungsfähigkeit gegenüber neuen oder veränderten Krankheitserregern aus. Außerdem merkt sich durch sie unser Körper den ersten Kontakt mit Keimen. Es kommt zur Ausbildung eines immunologischen Gedächtnisses. Das hat den Vorteil, dass die Immunabwehr bei erneuten Infektionen noch schneller darauf reagieren kann.
Das spezifische Immunsystem und die T-Helferzellen
Die Aufgabe des spezifischen Immunsystems ist es sowohl, fremde Erreger von außen zu erkennen und abzuwehren als auch krankhafte Veränderungen unserer eigenen Körperzellen zu erkennen und zu eliminieren. Das sind zwei völlig unterschiedliche Aufgaben, für die es spezialisierte Zellen braucht: die Lymphozyten-Abwehrzellen.
Eine Untergruppe hiervon sind die T-Helferzellen (TH0). Sie stellen quasi die zentrale Regulationseinheit unseres spezifischen Immunsystems dar. Sie werden anhand der von ihnen ausgeschütteten Zytokine (Botenstoffe), in fünf Untergruppen eingeteilt, die verschiedene und zum Teil gegensätzliche Funktionen haben.
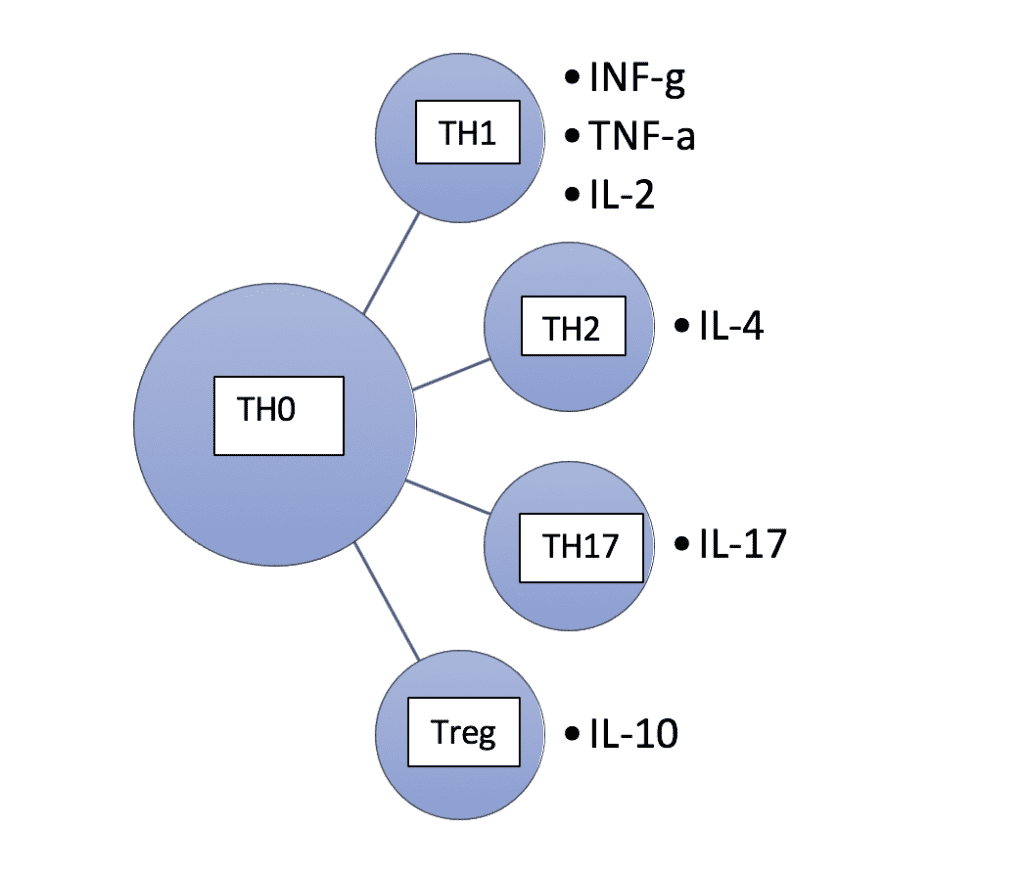
Aus TH0-Zellen können sich nach dem ersten Antigenkontakt TH1-, TH17-, TH2- und Treg-Zellen entwickeln. Deren Zusammenspiel ist sehr wichtig für eine effiziente und gut kontrollierte Immunreaktion.
Im Folgenden werden wir uns hauptsächlich mit den TH1- und den TH2-Zellen beschäftigen.
Was machen TH1-Zellen?
Die TH1-Zellen sorgen dafür, dass sich intrazelluläre Erreger (Viren) oder auch krankhaft veränderte Körperzellen (durch Krebs) nicht weiter vermehren können. Sie lösen den Zelltod solcher krankhaft veränderten oder infizierten Körperzellen aus. Das gelingt, indem die TH1-Zellen bestimmte Botenstoffe (Zytokine) ausschütten, die Fresszellen (Makrophagen) anlocken und aktivieren.
Die TH1-spezifischen Zytokine sind:
- Interferon-gamma (INF-g)
- Tumornekrosefaktor alpha (TNF-a)
- Interleukin-2 (IL-2)
Was passiert, wenn die TH1-Aktivität zu hoch reguliert wird?
Der Angriff der Fresszellen richtet sich dann nicht mehr nur gegen körperfremdes und krankhaft verändertes Zellmaterial, sondern auch gegen völlig gesunde körpereigene Zellen. Die TH1-Zellen sind dann nämlich nicht mehr in der Lage, die eigenen Körperzellen wiederzuerkennen. Sie verwechseln sie mit fremden Antigenen und lösen fälschlicherweise den Zelltod aus.
Eine erhöhte TH1-Aktivität findet man daher häufig bei Autoimmunerkrankungen:
- Hashimoto Thyreoiditis
- Morbus Basedow
- Multiple Sklerose
- Diabetes Mellitus Typ 1
- Rheumatoide Arthritis
- Psoriasis
- Morbus Crohn
Was machen TH2-Zellen?
TH2-Zellen sind für die Abwehr von extrazellulären Krankheitserregern zuständig. Dazu gehören Bakterien, Pilze und Parasiten. Sie besiedeln Schleimhäute, Blut, Gewebe und Zellzwischenräume. Im Gegensatz zu Viren sind diese Mikroorganismen eigenständige Organismen und benötigen keine Wirtszellen, um sich zu vermehren. Deshalb muss der Körper in diesem Fall auch keine eigenen Zellen zerstören, sondern konzentriert sich auf die Abwehr außerhalb der Zellen (extrazellulär).
TH2-Zellen sind ebenfalls verantwortlich für allergische Reaktionen. Diese Immunreaktionen werden eingeleitet, wenn die Zelloberflächen von eigentlich harmlosen Substanzen wie Pollen, Tierhaaren oder Nahrungsmitteln als gefährliche Antigene eingestuft werden.
Eine erhöhte TH2-Aktivität führt zu vermehrten allergischen Reaktionen
Ist die Aktivität von TH2 hochreguliert, lässt sich das in erster Linie an dem entzündungsfördernden Zytokin Interleukin-4 (IL4) im Blutbild ablesen. Die Kettenreaktion ist wie folgt:
IL4 stimuliert B-Zellen
↳ diese fördern die Synthese von IgE-, IgG1- und IgG3-Antikörpern
↳ diese wiederum passen zu den zuvor identifizierten „Fremdkörpern“
↳ dadurch werden Fresszellen angelockt (Granoluzyten), die den
Antigen-Antikörper-Komplex „auffressen“ (phagozytieren).
Typische Krankheitsbilder in Folge einer TH2-Dominanz sind:
- Asthma
- Neurodermitis
- Heuschnupfen
- Allergien
- Nesselsucht
- Nahrungsunverträglichkeiten IgE Typ und IgG1 Typ
- Histaminunverträglichkeit
- Mastzellaktivierungssyndrom
- Leaky Gut Syndrom
- Lupus Erythematodes
- Bestimmte Tumore
- viele chronisch-entzündliche Erkrankungen in der Spätphase
Mit zunehmendem Alter und unter bestimmten Gegebenheiten findet häufig ein TH2-Switch statt
Ein Hauptfaktor dafür ist Stress: Dazu zählt psychischer Stress aber auch starke körperliche Belastung, Fehlernährung, Nährstoffmängel, Alkohol, Nikotin, Umwelttoxine, Medikamente und Schwermetalle führen zu vermehrtem Zellstress.
Auch eine Schwangerschaft bewirkt einen TH2-Shift, weil dadurch ein Abstoßen des Fötus durch eine TH1-bedingte Immunantwort der Mutter verhindert werden soll. Das ist auch der Grund, weshalb sich während einer Schwangerschaft häufig Allergiesymptome verstärken und die Symptome einer Autoimmunerkrankung temporär verbessern. Gleichzeitig ist bei einer vorgeburtlichen TH1-Dominanz die Neigung zu Fehlgeburten höher und die Frauen haben es manchmal schwerer, schwanger zu werden.
TH1- und TH2-Zellen sollten idealerweise im Gleichgewicht sein
Da die TH1- und TH2-Zellen gegeneinander antagonistisch wirken, das heißt sich gegenseitig in ihrer Funktion hemmen, geht eine TH2-Dominanz in der Regel mit einer Schwächung der TH1-Immunantwort einher und umgekehrt. Ein Lösungsansatz besteht deshalb darin, die jeweils schwächere Seite zu stärken, um eine Balance wiederherzustellen.
Substanzen, welche die TH1-Antwort stimulieren können:
- Astragalus
- Ashwaganda
- Echinacea
- Zitronenmelisse
- Granatapfel
- Grapefruitkernextrakt
- Schwarzkümmelöl
- Selen
- Zink
- Arginin
- Cimetidin
- DHEA
- Glutamin
- Reishi
Substanzen, welche die TH2-Antwort stimulieren können:
- Koffein
- Grüntee-Extrakt
- Pinienrinden-Extrakt
- Silberweiden-Extrakt
- Lycopin
- Resveratrol
- Kiefernrindenextrakt
- Omega-3-Fettsäuren
- Curcumin
- Bromelain
- Boswellia
- Cannabis Sativa
Substanzen, die immunregulierend wirken und sowohl bei TH1- als auch bei TH2-Dominanz helfen können
- Vitamin A, C, E, D
- Probiotika
- Glutathion
- Omega-3-Fettsäuren
- Ginseng
- Curcumin
Was können wir aus dem TH1/TH2-Modell ableiten?
Als Beispiel nehme ich gern die beiden Hautkrankheiten Neurodermitis und Psoriasis. Auf den ersten Blick haben sie viel gemeinsam: das kranke Immunsystem äußert sich durch eine Erkrankung der Haut. Daher werden sie in der Regel auch als Hautkrankheiten eingestuft und entsprechend behandelt.
Sie unterscheiden sich aber grundlegend in der Art der vom Immunsystem ausgeschütteten Entzündungsmediatoren, den Zytokinen. Das bedeutet, was einem Neurodermitiker hilft, muss nicht zwangsläufig bei Psoroasis helfen und umgekehrt.
Was außerdem wichtig ist: Wenn ich an einer Autoimmunerkrankung leide, sollte ich vorsichtig sein mit Substanzen, welche die TH1-Antwort stimulieren. Das könnte nämlich zu einer Verschlechterung der Symptome führen, wenn das angeheizte Immunsystem auf einmal noch mehr Antikörper gegen körpereigenes Gewebe produziert. Auf der anderen Seite habe ich dann die Möglichkeit, durch TH2-Stimulation meine Symptome zu verbessern. So hat sich zum Beispiel Weihrauch-Extrakt (Boswellia), ein potenzielles TH2-Stimulans, in einigen Studien als hilfreich bei entzündlichen Darmerkrankungen und rheumatoider Arthritis gezeigt.
Allergiker und Atopiker profitieren häufig von Schwarzkümmelöl und sollten unbedingt auf einen guten Spiegel an Zink, Selen und Vitamin C achten. Koffein und Grüntee-Extrakt sind eher kontraproduktiv, weil sie den Cortisolspiegel erhöhen und zum TH2-Shift beitragen.
Grenzen des TH1/TH2-Modells
Die Vorgänge im Körper sind natürlich wesentlich komplexer, als es sich mit einem so einfachen Modell veranschaulichen lässt. Außerdem wurden hierbei zwei wesentliche Faktoren noch nicht berücksichtigt und zwar die Rolle der Treg– und der TH17-Zellen. Zur Erinnerung: auch sie entstehen durch Differenzierung von TH0-Zellen und sind am Gleichgewicht der Immunreaktion beteiligt.
Auch Treg- und TH17-Zellen sollten im Gleichgewicht sein
Treg-Zellen (regulatorische T-Zellen) sind wichtig für die Aufrechterhaltung der Immuntoleranz. Sie verhindern unerwünschte oder überschießende Immunreaktionen auf körpereigene Strukturen im Körper. Man kann sie auch als „Bremse“ des Immunsystems betrachten.
TH17-Zellen wurden so genannt, weil sie das Zytokin IL-17 bilden. In den letzten Jahren hat man herausgefunden, dass TH17-Lymphozyten ähnlich wie TH1-Zellen ebenfalls eine wichtige Rolle in der Entwicklung chronisch-entzündlicher Erkrankungen, einschließlich multipler Sklerose, Psoriasis, entzündlicher Darmerkrankungen, Hashimoto-Thyreoiditis und rheumatoider Arthritis spielen.
Es kann also durchaus sein, dass du, solltest du an einer Autoimmunerkrankung leiden, gar keine TH1-Dominanz hast, sondern einen Überschuss an TH17-Zellen. Dann macht eine Immunmodulation im Sinne der Stimulierung von Treg-Zellen mehr Sinn als die Stimulierung von TH2.
In diesem Zusammenhang werden vor allem Curcumin und Vitamin D untersucht. Auch verschiedene Probiotika-Stämme können vermutlich einen Mangel an Treg-Zellen ausgleichen.
Was macht die Schulmedizin?
In der Medizin wurden insbesondere in den letzten Jahren vermehrt sogenannte monoklonale Antikörper entwickelt. Sie unterdrücken das Immunsystem, indem sie entweder TH1- oder TH2-spezifische Interleukine blockieren.
Adalimumab, Certolizumab, Etanercept, Golimumab und Infliximab blockieren TNF-a und werden bei Rheumatoider Arthritis, Psoriasis-Arthritis, Morbus Crohn, Colitis ulcerosa und Morbus Bechterew eingesetzt.
Die beiden Antikörper Secukinumab und Ixekizumab richten sich gegen Interleukin-17A und wurden zur Behandlung der Psioriasis entwickelt.
Dupilumab blockiert IL-4 und IL-13 und wirkt dadurch gegen Neurodermitis und Asthma bronchiale.
Das sind nur einige Beispiele.
Der Vorteil dieser Antikörper ist, dass sie sehr spezifisch nur bestimmte Reaktionen des Immunsystems ausschalten und nicht unselektiv das komplette Immunsystem unterdrücken, wie es zum Beispiel bei Kortikosteroiden der Fall ist.
Der Nachteil ist, dass die meisten Antikörper erst seit relativ kurzer Zeit auf dem Markt sind. Daher sind mögliche Langzeitnebenwirkungen noch unbekannt. Je nachdem welche Interleukine blockiert werden, steigt das Risiko für Infektionen mit Viren, Parasiten, Bakterien oder Pilzen. Außerdem kann es bei Unterdrückung der TH1-Immunantwort sein, dass auch das Risiko für Tumorerkrankungen ansteigt, denn die TH1-Zellen sorgen ja normalerweise dafür, dass sich intrazelluläre Erreger und auch krankhaft veränderte Körperzellen nicht weiter vermehren können.
Wie finde ich heraus, was mir hilft?
Bei jeder Art von chronischer Entzündung ist eine antientzündliche Ernährung die wichtigste Basis. Denn: viele sekundäre Pflanzenstoffe und Mikronährstoffe wirken ausgleichend und harmonisierend auf dein Immunsystem – und das ohne Nebenwirkungen.
Antientzündliche Ernährung – Tschüss Müdigkeit, hallo Energie!
Endlich wieder richtig gut fühlen – Mein Onlinekurs hilft dir dabei! Wissenschaftlich fundiert und mit nachgewiesenen Erfolgen: Der Kurs ist zertifiziert, wurde erfolgreich evaluiert und wird mit bis zu 100€ von den Krankenkassen bezuschusst.

Darüber hinaus können bestimmte Naturstoffe als Ergänzung dabei helfen, die Immuntoleranz wieder herzustellen. Dabei hemmen sie ähnlich wie bestimmte Medikamente, die schulmedizinisch eingesetzt werden, entzündliche Interleukine aber weniger stark und dementsprechend mit weniger Nebenwirkungen.
Dazu muss allerdings gesagt sein, dass die Evidenz noch ausbaufähig ist, sprich: es fehlen in der Regel groß angelegte Humanstudien (RCTs), welche die Wirksamkeit belegen. Das ist bei Naturstoffen leider so gut wie immer der Fall, weil solche Studien sehr teuer und aufwendig sind und selten von großen Unternehmen oder anderen Institutionen finanziell unterstützt werden.
Ich hoffe, mein kleiner Einblick in die Immunologie hat dir gefallen und dir ein besseres Verständnis für die Vorgänge in deinem Körper ermöglicht.
Quellen
Quellen
Akdis, C. und Akdis, M. (2014): Mechanism of immune tolerance to allergens: Role of IL-10 and Tregs. The Journal of Clinical Investigation, 124(11): 4678–4680.
Bacher, P. et al. (2016): Regulatory T Cell Specificity Directs Tolerance versus Allergy against Aeroantigens in Humans. Cell, 167(4): 1067-1078.
Berker, M. et al. (2016): Allergies – A T celle perspective in the era beyond the TH1/TH2 paradigm. Clinical Immunology, 12(174): 73-83.
Hirahara, K. und Nakayama, T. (2016): CD4+ T-cell subsets in inflammatory diseases.: beyond the TH1/Th2 paradigm. International Immunology, 28(4): 163-171.
Noval Rivas, M. et al. (2016): Regulatory T cells in allergic diseases. Journal of Allergy & Clinical Immunology, 138(3): 639-652.
Oalomares, O. et al. (2014): Regulatory T cells and immune regulation of allergic diseases: roles of IL-10 and TGF-β. Genes & Immunity, 15: 511-520.
Ulgres, A. et al. (2015): Protein kinas CK2 enables regulatory T cells to suppress excessive TH2 responses in vivo. Nature Immunology, 16: 267-275.
Borish LC, et al (1999): Interleukin-4 receptor in moderate atopic asthma. A phase I/II randomized, placebo-controlled trial. Am J Respir Crit Care Med 160: 1816-1823.
G. Chaouat, E. Menu, R. Kinsky, C. Brezin (1990): Immunologically mediated abortions: one or several pathways? Research in Immunology, 141(2): 188-192.
Zenclussen A.C., Blois, S., Stumpo, R. et al. (2003): Murine abortion is associated with enhanced interleukin-6 levels at the feto-maternal interface. Cytokine, 24(4):150‐160.
Zenclussen, A.C., Fest, S., Busse, P., Joachim, R., Klapp, B.F., Arck, P.C. (2002): Questioning the Th1/Th2 paradigm in reproduction: peripheral levels of IL-12 are down-regulated in miscarriage patients. Am J Reprod Immunol, 48(4):245‐251.
Ishikura, H., Fukui, H., Takeyama, N., Tanaka, T. (1993): Cimetidine activates interleukin-12, which enhances cellular immunity. Blood, 199 (5): 1782-3.
Nestle, F. O., et al. (1994): Characterization of dermal dendritic cells in psoriasis. Autostimulation of T lymphocytes and induction of Th1 type cytokines. J. Clin. Invest. 94: 202 – 209.
Ghoreschi, K., et al. (2003): Interleukin-4 therapy of psoriasis induces Th2 responses and improves human autoimmune disease. Nat. Med. 9: 40 – 46.
Brush, J., Mendenhall, E., Guggenheim, A., Chan, T., Connelly, E., Soumyanath, A., Buresh, R., Barrett, R., Zwickey, H. (2006): The effect of Echinacea purpurea, Astragalus membranaceus and Glycyrrhiza glabra on CD69 expression and immune cell activation in humans. Phytother Res, 20: 687–95 .
Calder, P.C. (1994): Review: Glutamine and the immune system. Clin Nutrition 13:2–8.
Correale J. et al. (2009): Immunmodulatory Effects of Vitamin D in Multiple Sclerosis. Brain, 132: 1126-7.
Munger K.L. et al. (2006): Serum 25-hydroxy-vitamin D Levels and Risk of Multiple Sclerosis. JAMA, 296: 2832-8.
Hatcher, H., Planalp, R., Cho,. J, et al. (2008): Curcumin: From ancient medicine to current clinical trials. Cell Mol Life Sci, 65:1631–1652.
Perricone, C., De Carolis, C. , Perricone, R. (2009): Glutathione: A key player in autoimmunity. Autoimmunity Rev, 8:697–701.
Rode von Essen, M., Kongsbak, M., Schjerling, P. et al. (20210): Vitamin D controls T cell antigen receptor signaling and activation of human T cells. Nature Immunol, 11(4): 344–50.
Wang, J., Su, B., Ding, Z., Du, X., Wang, B. (2008): Cimetidine enhances immune response of HBV DNA vaccination via impairment of the regulatory function of regulatory T cells. Biochem Biophys Res Comm, 372: 491–96.
Leung, S. et al. (2010): The cytokine milieu in the interplay of pathogenic Th1/ Th17 cells and regulatory T cells in autoimmune disease. Cellular & Molecular Immunology 7: 182–189.
Lee G. R. (2018). The Balance of Th17 versus Treg Cells in Autoimmunity. International journal of molecular sciences, 19(3): 730.